高二化学期末考试重点知识点(高二化学必看期末考复习知识点及技巧大全)

文 : 网络 如有侵权请联系我们删除。图:互联网。如有转载,请联系并注明原出处!
资料已备好,还不行动起来!
第一章、化学反应与能量
考点1:吸热反应与放热反应
1、吸热反应与放热反应的区别
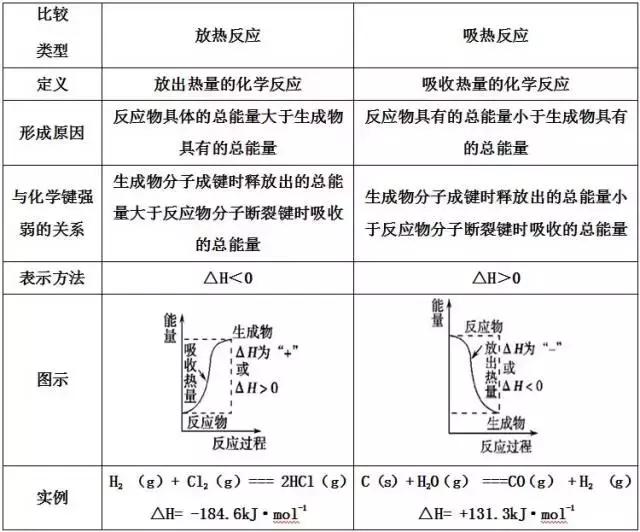
完整版请在自主招生zzzs010查看
特别注意:反应是吸热还是放热与反应的条件没有必然的联系,而决定于反应物和生成物具有的总能量(或焓)的相对大小。
2、常见的放热反应
等也是吸热反应;
④水解反应
考点2:反应热计算的依据
1.根据热化学方程式计算
反应热与反应物各物质的物质的量成正比。
2.根据反应物和生成物的总能量计算
ΔH=E生成物-E反应物。
3.根据键能计算
ΔH=反应物的键能总和-生成物的键能总和。
4.根据盖斯定律计算
化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关。即如果一个反应可以分步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的。
温馨提示:
①盖斯定律的主要用途是用已知反应的反应热来推知相关反应的反应热。
②热化学方程式之间的“ ”“-”等数学运算,对应ΔH也进行“ ”“-”等数学计算。
5.根据物质燃烧放热数值计算:Q(放)=n(可燃物)×|ΔH|。
第二章、化学反应速率与化学平衡
考点1:化学反应速率
1、化学反应速率的表示方法___________。
化学反应速率通常用单位时间内反应物浓度和生成物浓度的变化来表示。表达式:___________ 。
其常用的单位是__________ 、 或__________ 。
2、影响化学反应速率的因素
1)内因(主要因素)
反应物本身的性质。
2)外因(其他条件不变,只改变一个条件)

3、理论解释——有效碰撞理论
(1)活化分子、活化能、有效碰撞
①活化分子:能够发生有效碰撞的分子。
②活化能:如图

图中:E1为正反应的活化能,使用催化剂时的活化能为E3,反应热为E1-E2。(注:E2为逆反应的活化能)
③有效碰撞:活化分子之间能够引发化学反应的碰撞。
(2)活化分子、有效碰撞与反应速率的关系

考点2:化学平衡
1、化学平衡状态:一定条件(恒温、恒容或恒压)下的可逆反应里,正反应和逆反应的速率相等,反应混合物(包括反应物和生成物)中各组分的浓度保持不变的状态。
2、化学平衡状态的特征

3、判断化学平衡状态的依据

免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。






